Kirsten Rat Sarcoma virusni onkogenski homolog (KRAS) je najčešće mutirani podtip porodice RAS i nekada se smatrao metom "nelijekom". Poslednjih godina, inhibitori kovalentnih mutacija koji ciljaju mutaciju KRASG12C napravili su značajan napredak, a dva inhibitora malih molekula, AMG510 (Sotorasib) i MRTX849 (Adagrasib), sukcesivno su odobreni od strane američke FDA, što je pokrenulo talas istraživanja o lekovi koji ciljaju na KRAS koji se teško uzima u obzir. Međutim, na tržištu još uvijek nema lijekova za mutacije osim KRASG12C, posebno KRASG12D, koji je široko rasprostranjen u mnogim tumorima, a nedavno je Miratijev MRTX1133, kao prvi oralno reverzibilni inhibitor KRASG12D, upravo ušao u fazu I, koja je uvelike podstakao istraživanje o lijekovima koji ciljaju ovu mutaciju.
Nedavno su istraživački tim Zhang Aoa sa Farmaceutskog fakulteta, Šangajskog univerziteta Jiaotong i istraživački tim Pang Xiu-fenga sa School of Life, East China Normal University, blisko sarađivali kako bi postigli napredak u proučavanju malih molekula protiv tumora. inhibitori koji ciljaju mutaciju KRASG12D. Rad je nedavno objavljen online u međunarodno priznatom akademskom časopisu Journal of Medicinal Chemistry: https://doi.org/10.1021/acs.jmedchem.3c01724.
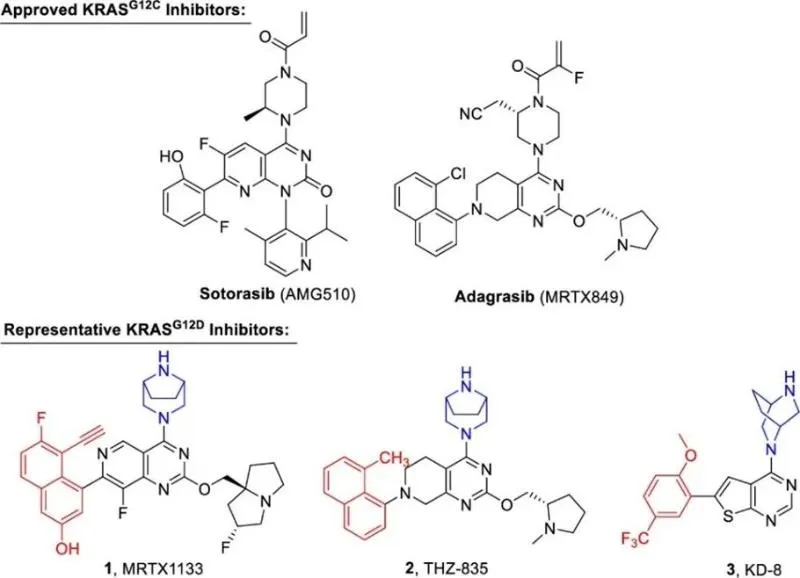
U ovoj studiji, zasnovanoj na kristalnoj strukturi kompleksa MRTX1133, istraživači su izvršili sistematsku strukturnu optimizaciju regiona P petlje okupiranog osnovnim fragmentom azetidinijumovog premosnog prstena, hidrofobnim džepom na levoj strani molekula gde je naftalenski prsten u interakciji. , i oblast rastvarača u kojoj pirolizidinski biciklični prsten interaguje, s jedne strane. Konkretno, izvršena je deuteracija benziloksimetilena, potencijalnog metaboličkog mjesta, kako bi se povećala stabilnost jedinjenja, dok je uvođenje sidodifluorolefinskog supstituenta povećalo novost molekula, što je rezultiralo klasom pirolizidin deuteriranih spojeva sa supstituentima sidodifluoroolefina. i 28.
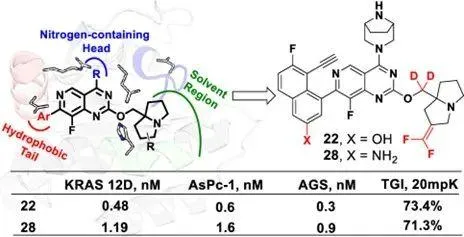
Slika 2. Strukturni dizajn lijeka novog KRAS-aG12Dinhibitori.
Jedinjenja 22 i 28 su pokazala nizak nanomolarni nivo (0.3 - 1.6 nM) inhibitornu aktivnost protiv ćelijskih linija kao što su AsPc-1 i AGS koji eksprimiraju mutaciju KRASG12D, i slabiju aktivnost protiv drugih KRASG12S mutantni soj A549 kao i ćelije KRASWT H1299, pokazujući bolju selektivnost za KRASG12D. Nakon toga, utvrđeno je da su jedinjenja veoma aktivna u inhibiciji interakcija RAF-RAS proteina na molekularnom nivou konstruiranjem homogenog testa zasnovanog na vremenski razlučivoj fluorescenciji (HTRF) (IC50=0.48 - 1.19 nM). Nadalje, u ljudskim ćelijama raka pankreasa AsPc-1 i ćelijama raka crijeva AGS, nova jedinjenja su dozno-ovisna i značajno inhibirala fosforilaciju KRAS nizvodnih proteina ERK i AKT. Protočna citometrijska analiza je takođe pokazala da je procenat apoptotičkih ćelija nakon 24 sata tretmana ovim jedinjenjima (50 nM) bio približno dva puta veći nego u slepoj kontrolnoj grupi. U AsPC-1 mišjem modelu tumorskog tumora ksenografta, nova jedinjenja su postigla 73,4% i 71,3% inhibiciju rasta tumora (TGI) pod intraperitonealnom primjenom od 20 mg/kg dva puta dnevno, respektivno, dok nije bilo značajne promjene u tjelesne težine miševa. Western-Blot analiza tumorskog tkiva pokazala je da nova jedinjenja značajno inhibiraju fosforilaciju KRAS nizvodnih proteina ERK i AKT in vivo. Uzeto zajedno, ovo sugerira da ova klasa spojeva ima dobru sigurnost i antitumorsko djelovanje s potencijalom za dalja istraživanja.
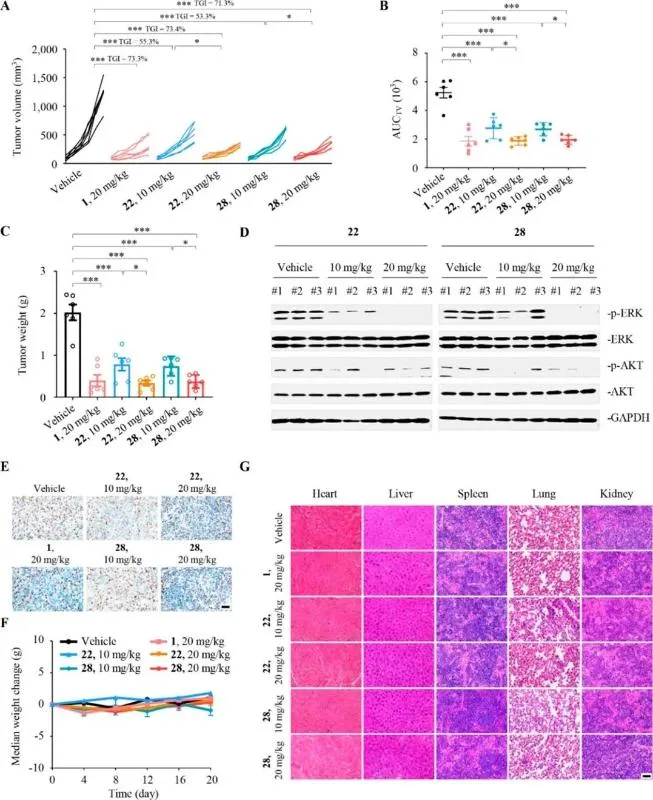
Slika 3. Antitumorski efekti jedinjenja u mišjim modelima tumorskog ksenografta in vivo.






